أدت التطورات الحديثة في تكنولوجيا تصنيع العمود الكروماتوغرافي ، وتحسين الأدوات ، وتصميم الكاشف ، وتحليل البيانات إلى تطور كبير في مجال الكروماتوغرافيا.
يعتبر الكروماتوغرافيا السائلة فائق الأداء مجالًا جديدًا في علم الفصل ، والذي ، بالإضافة إلى الحفاظ على مبادئ كروماتوغرافيا السائل عالية الأداء ، قد حسّن بشكل كبير القدرات الثلاث للسرعة والحساسية والفصل. في الجهاز الذي يستخدم هذه التقنية ، يتم استخدام جزيئات أصغر من HPLC (أقل من µm2.5) ؛ لذلك ، يتم تقليل طول العمود ، ويتم إجراء التحليل في وقت أقصر ، كما يتم تقليل استهلاك المذيبات.
تتضمن هذه المقالة العناوين التالية:
1 المقدمة
2- كيمياء جسيمات حشو العمود
3- الأجهزة
4- تطبيقات الكروماتوغرافيا السائلة بكفاءة غير عادية
1-4- زيادة سرعة التحليل وفصل القمم
2-4- تحليل المركبات الطبيعية والأدوية العشبية
3-4- دراسات التحليل الحيوي
4-4- تحديد كمية الشوائب
5-4- العيوب
5-خاتمة.
1- المقدمة
خلال الثلاثين عامًا الماضية وحتى اليوم ، يعد الكروماتوغرافيا السائلة عالية الأداء إحدى التقنيات الكروماتوغرافية الرئيسية المستخدمة في المعامل حول العالم ، وأحد أسباب توسع هذه الطريقة هو تطوير مواد لملء الأعمدة الكروماتوغرافية ، والتي تحتوي على تأثير كبير على الانفصال. تتمثل إحدى القيود الرئيسية لـ HPLC في افتقاره إلى الكفاءة مقارنةً بالكروماتوغرافيا الغازية أو الرحلان الكهربائي الشعري(Capillary electrophoresis) بسبب انخفاض معامل التوزيع في الطور السائل ، مما يبطئ تغلغل التحليل في المرحلة الثابتة. أساس UPLC هو استخدام مرحلة ثابتة بحجم جسيم أقل من 2 ميكرومتر ، مقارنة بـ HPLC ، الذي يتراوح حجم جسيمه بين 3-5 ميكرومتر.
يمكن تفسير تأثير جسيمات حشو العمود بواسطة معادلة فان ديميتر ، المألوفة لكل من يعرف مبادئ الكروماتوغرافيا [1]. معادلة فان ديميتر هي صيغة تجريبية توضح العلاقة بين السرعة الخطية (سرعة التدفق) وارتفاع اللوحة (كفاءة العمود). نظرًا لأن حجم الجسيمات هو أحد المتغيرات ، يمكن استخدام منحنى Van Dimeter للتحقق من كفاءة اللوني (الشكل 1). تُظهر معادلة فان ديميتر المكونة من ثلاثة مكونات أن نطاق معدلات التدفق للأداء الجيد مع أقطار الجسيمات الأصغر أكبر بكثير من نطاق الجسيمات الأكبر [2 ، 3].
H=A+B/U+CU
في هذه المعادلة ، A و B و C ثابتة و U: السرعة الخطية. الثابت A مستقل عن السرعة ويمثل التیار الدوامي. يكون هذا التعبير عند قيمته الأدنی عندما تكون مواد تعبئة العمود صغيرة وموحدة. يمثل الثابت B اتجاه الانتشار الطبيعي لجزيئات العينة. يتم إزالة هذا التأثير بسرعات عالية وبالتالي يتم تقسيمه على سرعة التدفق (U).أصل ثابت C هو المقاومة الحركية للتوازن في عمليات الفصل. المقاومة الحركية هي التأخير في الانتقال من الطور المتحرك إلى الطور الثابت و بالعكس. كلما زاد معدل تدفق الطور المتحرك ، كلما زاد ميل الجزيء الموجود في الطور الثابت إلى التخلف عن الجزيء في الطور المتحرك ، لذلك يتناسب هذا الثابت مع معدل التدفق (U).
تُظهر معادلة Van Dimter أن الكفاءة تتحسن مع وجود جزيئات أصغر ، ولكن في الوقت نفسه ، تؤدي الجسيمات الأصغر إلى ارتفاع ضغط الظهر ، بينما تعمل معظم أجهزة HPLC حتى ضغط bar400 فقط. لهذا السبب ، يمكننا أن نفهم سبب استخدام أعمدة أقصر مع جسيمات أصغر من µm2 ؛ لأنه بهذه الطريقة فقط تزداد سرعة التحليل دون فقدان الكفاءة. لذلك ، من الممكن زيادة قدرة وسرعة التحليل دون التأثير على كفاءة الكروماتوغرافيا. أدى ظهور UPLC إلى تطوير جهاز كروماتوغرافيا سائلة حيث يجب تقليل الحجم الميت ومقاومة الضغوط من psi15000 إلى 8000 رطل لكل بوصة مربعة. الكفاءة تتناسب مع حجم الجسيمات وتتناسب عكسيا مع طول العمود. لهذا السبب ، يصبح العمود أقصر مع تناقص حجم الجسيمات.
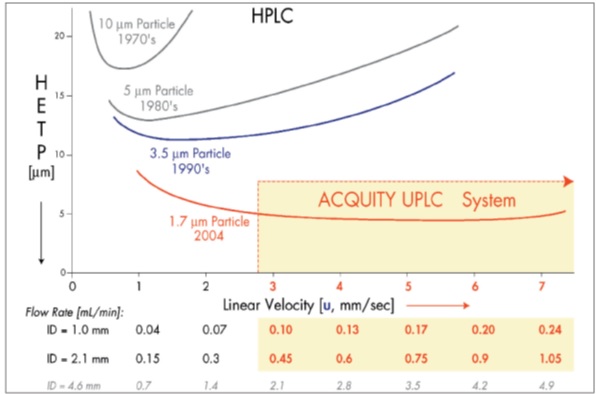
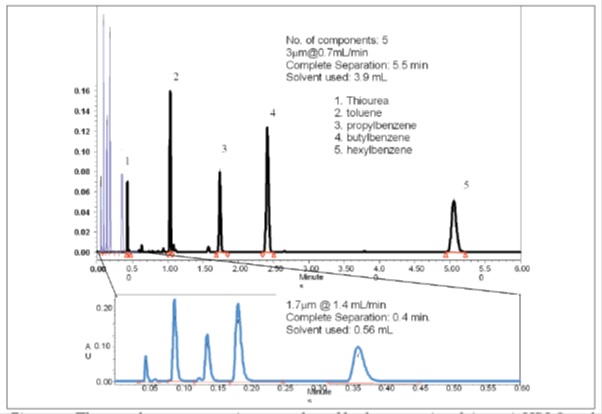
استنادًا إلى نظرية HPLC ، مع انخفاض حجم مادة تعبئة العمود ، تزداد الكفاءة والدقة. يوضح الشكل (1) أنه عندما يكون حجم الجسيمات أقل من 3.5 ميكرومتر ، لا يتم الحصول على كفاءة عالية فقط ، ولكن لا يتم فقدان هذه الكفاءة عند معدلات التدفق العالية. باستخدام جزيئات أصغر ، يمكن دفع السرعة والسعة القصوى (عدد القمم المفصولة لكل وحدة زمنية) إلى حدود جديدة تسمى كروماتوغرافيا السائل فائقة الأداء ، أو UPLC. باستخدام UPLC ، أصبح من الممكن الآن الاستفادة من كل قوة الكروماتوغرافيا للفصل باستخدام أعمدة أقصر أو معدلات تدفق أعلى – من أجل تحقيق سرعات أعلى مع فصل وحساسية أكبر بكثير. يمكن رؤية مفهوم UPLC بشكل أكثر تحديدًا في الشكل (2) ، والذي يقارن فصل خمسة مركبات في خليط مع HPLC و UPLC. إن مخطط الكروماتوجرام السفلي عبارة عن تراكب عريض يبلغ 0/6 دقيقة للكروماتوجرام العلوي يوضح زيادة سرعة الفصل في UPLC.
2- كيمياء جسيمات حشو العمود
يعد تصميم وتطوير جسيمات أصغر من µm2 تحديًا أساسيًا ويتم إجراء بحث مكثف من قبل الباحثين في هذا المجال [4]. على الرغم من أن الجسيمات غير المسامية الفعالة بحجم µm1/5 متوفرة تجارياً ، إلا أن هذه الجسيمات لها مساحة سطح صغيرة ، مما يؤدي إلى انخفاض قدرة التحميل والتثبيط. للحفاظ على القدرة والتثبيط المماثل لـ HPLC ، يجب أن تستخدم طريقة UPLC جزيئات مسامية جديدة يمكنها تحمل الضغوط العالية. تتمتع الجزيئات القائمة على السيليكا بقوة ميكانيكية جيدة ، ولكن لها أيضًا عيوب. من بين هذه العيوب ، يمكننا أن نشير إلى عزل التحليلات الأساسية وقابلية التطبيق في نطاق صغير من الأس الهيدروجيني. البديل الآخر هو أعمدة البوليمر التي تعمل في نطاق أوسع من pH، ولكن لها أيضًا عيوب مثل الكفاءة المنخفضة والقدرات المحدودة.
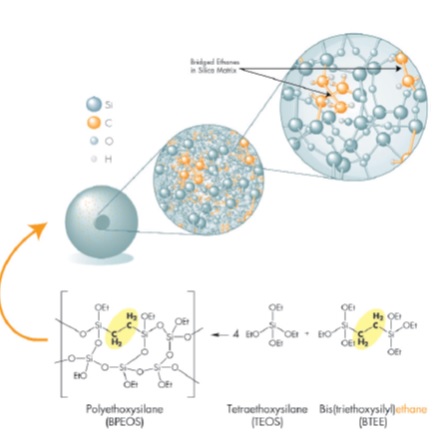
في عام 2000 ، قدمت Waters Company الجيل الأول من العمود Hybrid المسمى Xtra ، والذي كان يتمتع بمزايا كل من أعمدة السيليكا والبوليمر. تتمتع هذه الأنواع من الأعمدة بقوة ميكانيكية أعلى بالإضافة إلى أداء في نطاق أوسع من pH. يتم تصنيع أعمدة Xtra باستخدام تخليق سول-جل الكلاسيكي ، والذي يدخل الكربون في الهيكل في شكل الميثيل. بالطبع ، من أجل توفير الطاقة الميكانيكية المطلوبة للجيل الثاني من جهاز UPLC ، تم تقديم تقنية هجينة ، والتي سميت ACQUITY UPLC [5]. تربط جزيئات ACQUITY بحجم µm1/7 مجموعات الميثيل في مصفوفة السيليكا من خلال جسر ، كما هو موضح في الشكل (3) ، مما يزيد من الاستقرار الميكانيكي للجسيمات.
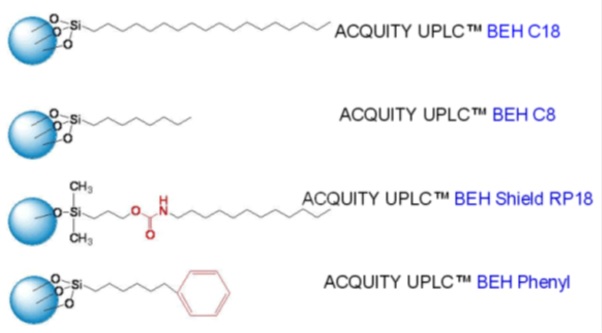
هناك أربع مراحل ثابتة لـ ACQUITY لفواصل UPLC:
- (أعمدة سلسلة Alkyl المستقيمة) ACQUITY UPLCTM BEH C18؛
- (أعمدة سلسلة Alkyl المستقيمة) C8 ACQUITY UPLCTM BEH؛
- (الأعمدة ذات المجموعات القطبية) ACQUITY UPLC BEH Shield RP18 ؛
- ترتبط مجموعة فينيل بمجموعة silyl من خلال سلسلة من 6 كربون ACQUITY UPLC BEH Phenyl.
يوفر كل عمود مجموعة من العوامل المختلفة مثل مقاومة الماء ونشاط السيلانول واستقرار التحلل المائي والتفاعل الكيميائي مع المادة التحليلية (الشكل 4).
الأعمدة من النوع (1) و (2) المذكورة أعلاه هي أعمدة عالمية لمعظم أغراض فصل UPLC التي توفر أيضًا نطاقًا واسعًا منpH. في هذه الأنواع من الأعمدة ، تتسبب كيمياء روابط الترابط الثلاثي التكافؤ في ثبات ضئيل عند انخفاضpH. يتحد هذا الثبات المنخفض عند pH المنخفض مع الاستقرار عند pH العالي لجزيئات BEH 1.7 ميكرومتر لإنتاج أعمدة ذات ثبات في نطاق pH الأعلى. توفر الأعمدة من النوع (3) انتقائية مكملة لأعمدة من النوع (1) و (2). تستخدم الأعمدة من النوع (4) المذكورة أعلاه مجموعة الألكيل المكونة من 6 كربون ثلاثية الوظائف بين حلقة فينيل ومجموعة سيليل الوظيفية. يزيد هذا الترابط من عمر العمود ويعطي أشكال ذروة ممتازة. القطر الداخلي للعمود عادة ما يكون 1/2 مم. للوصول إلى الحد الأقصى من الدقة ، يبلغ طول العمود mm100، ولتحليل أسرع ، يناسب mm50 لطول العمود.
الأعمدة من النوع (1) و (2) المذكورة أعلاه هي أعمدة عالمية لمعظم أغراض فصل UPLC التي توفر أيضًا نطاقًا واسعًا منpH. في هذه الأنواع من الأعمدة ، تتسبب كيمياء روابط الترابط الثلاثي التكافؤ في ثبات ضئيل عند انخفاضpH. يتحد هذا الثبات المنخفض عند pH المنخفض مع الاستقرار عند pH العالي لجزيئات BEH 1.7 ميكرومتر لإنتاج أعمدة ذات ثبات في نطاق pH الأعلى. توفر الأعمدة من النوع (3) انتقائية مكملة لأعمدة من النوع (1) و (2). تستخدم الأعمدة من النوع (4) المذكورة أعلاه مجموعة الألكيل المكونة من 6 كربون ثلاثية الوظائف بين حلقة فينيل ومجموعة سيليل الوظيفية. يزيد هذا الترابط من عمر العمود ويعطي أشكال ذروة ممتازة. القطر الداخلي للعمود عادة ما يكون 1/2 مم. للوصول إلى الحد الأقصى من الدقة ، يبلغ طول العمود mm100، ولتحليل أسرع ، يناسب mm50 لطول العمود.
يعد ملء العمود بجزيئات µm1/7. بطريقة قابلة للتكرار أيضًا تحديًا يجب التغلب عليه. يجب أن يكون للأعمدة المبنية سطح داخلي أكثر نعومة ويجب تصميم جميع مكوناتها بطريقة تمنع العمود من الانسداد. يعد توحيد العمود مهمًا أيضًا ، خاصة بالنسبة للأعمدة الأقصر للحفاظ على الفصل أثناء الفصل بشكل أسرع.
3- الأجهزة
بشكل عام ، بالنسبة لأجهزة UPLC ذات التقنيات المتقدمة ، يجب أيضًا تصميم المضخة والحاقن التلقائي والكاشف ونظام البيانات. نظرًا لأن جزيئات تعبئة العمود أصغر ، يجب تطبيق نطاق ضغط أكبر لتحقيق عمليات فصل بقدرات ذروة أعلى من أجهزة HPLC التقليدية اليوم. انخفاض الضغط المحسوب بمعدل التدفق الأمثل والكفاءة القصوى في عمود 15 سم µm1/7 من الجسيمات يعادل psi15000. لذلك ، من الضروري وجود مضخة قادرة على تمرير المذيب بشكل موحد وقابل للتكرار عبر العمود عند هذا الضغط.
يعد إدخال العينة في العمود أيضًا عاملاً مهمًا وأساسيًا. لم يتم تصميم الحاقنات اليدوية أو الأوتوماتيكية الحالية للعمل في مثل هذه الضغوط العالية. للحفاظ على العمود من تقلبات الضغط ، يجب أن يكون الحقن عديم النبض قدر الإمكان. يجب أن يكون حجم مذيب الغسيل في أدنى حد له لمنع اتساع النطاق. يعد وقت الحقن السريع في جهاز UPLC في مقياس السرعة المقدم أحد الأشياء التي يجب مراعاتها. حجم الحقن المنخفض وحجم المذيبات المنخفض من العوامل التي تسبب حساسية عالية في UPLC.
مع الجسيمات التي يبلغ قطرها µm1/7. ، سيكون عرض الذروة عند نصف ارتفاع أقل من ثانية واحدة ، وهذه المشكلة تمثل أيضًا تحديًا مهمًا للكاشف. للحصول على قمم قياسية ذات قابلية استنساخ عالية ، يجب أن يكون الكاشف سريعًا بما يكفي لتسجيل المزيد من البيانات في أي لحظة. نتيجة لذلك ، ستكون حساسية طريقة UPLC أعلى بمرتين إلى ثلاث مرات من فصل HPLC التقليدي ، اعتمادًا على دقة أجهزة الكشف.
يوضح الجدول رقم (1) مقارنة بين مواصفات جهازي HPLC و UPLC.
| بیانات | HPLC | UPLC |
| حجم الجسیمات | 3-5µm | أقل من 2µm |
| أقصی ضغط خلفی | 35-40MPa | 103/5MPa |
| عمود تحلیلی | Alltima C18 | Acquity UPLC BEH C18 |
| عمود | mm3/2 × 150 | mm2/1 × 150 |
| درجة حرارة العمود | C˚30 | C˚65 |
| حجم الحقن | lµ2 | lµ2 |
4- تطبيقات الكروماتوجرافيا السائلة بكفاءة غير عادية
1-4زيادة سرعة التحليل وفصل القمم
غالبًا ما يضحي الأشخاص الذين يستخدمون الكروماتوغرافيا بالفصل من أجل السرعة. UPLC يتغلب على هذه المشاكل. في الشكل (5) ، فصل ثمانية مركبات بترتيب القمم ، أسيتازولاميد ، هيدروكلوروثيازيد ، شوائب ، هيدروفلوميثيازيد ، كلوباميد ، ترايكلورميثيازيد ، إنداباميد ، بندروفلوميثيازيد وسبيرونولاكتون (كل تركيز mg/ml0/1 في الماء) مع UPLC في أقل من يتم عرض 1/6 دقيقة بينما تم إجراء فصل مماثل في عمود بقطر 1.2 وطول 100 مم بعمود C18 وقطر جسيمي يبلغ mµ5 مع فاصل مماثل في عشر دقائق.
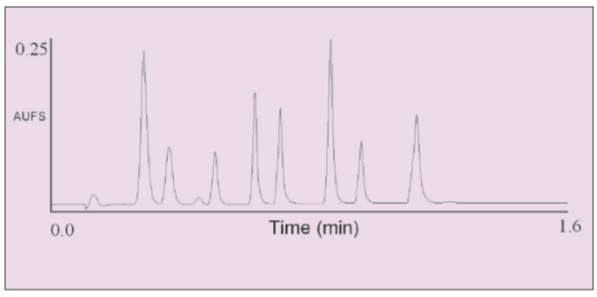
عمود قطره 1.2 مم ، طوله 30 مم مليء بجزيئات ACQUITY UPLC C18 بقطر 1.7 ميكرومتر عند 35 درجة مئوية. تدرج 9-45٪ في تدرج خطي خلال 0.8 دقيقة بمعدل تدفق ml/min0/86 المرحلة المتنقلة A (0/1 ٪ حمض الفورميك) ، B (أسيتونتريل). كشف UV عند nm273.
ولكن بالنسبة لبعض التحليلات ، تعتبر السرعة ذات أهمية ثانوية ويتم إعطاء الأولوية لقدرة الذروة والدقة. يوضح الشكل (6) فصل الببتيدات ، والهدف الرئيسي منها هو تعظيم عدد القمم. في هذا التطبيق ، تزداد سعة الذروة (عدد القمم المنفصلة في الدقيقة) في UPLC بشكل كبير.
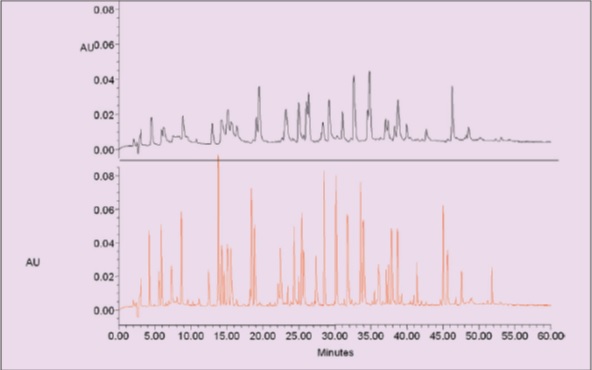
في الشكل (6) ، يوضح فصل الببتيدات باستخدام عمود HPLC و C18 و µm5 من الجسيمات ، مما يعطي سبعين قمة بسعة ذروة 143 ، بينما في الطيف السفلي حيث تم فصل الببتيدات بواسطة UPLC ، كانت النتيجة من 168 قمة مع توفر سعة ذروة 360 (زيادة 2.5 مرة).
2-4-تحليل المركبات الطبيعية والأدوية العشبية
يستخدم UPLC على نطاق واسع لتحليل المركبات الطبيعية والأدوية العشبية. تحتاج المعامل التحليلية إلى زيادة معرفتها في مجال علم الأدوية لتقديم أدلة تستند إلى فعالية الدواء وأيضًا لتوفير عوامل الأمان للمنتجات. الهدف الرئيسي في هذا المجال هو تحليل العينات الصيدلانية في مصفوفة معقدة. يتيح UPLC عزل وتحديد المركبات النشطة في عينات معقدة للغاية من المركبات الطبيعية والأدوية العشبية.
3-4- دراسات التحليل الحيوي
لغرض الدراسات السمية والدوائية ، يعد تحديد كمية الدواء في العينات البيولوجية جزءًا مهمًا من الدراسات. معظم الأدوية عبارة عن مركبات ذات وزن جزيئي منخفض ويتم اختبارها في الدراسات قبل السريرية والسريرية. يتم استخدام العديد من المصفوفات البيولوجية للتحليلات الكمية ، بما في ذلك الدم والبلازما والبول. الطريقة الأساسية في التحليل البيولوجي الكمي هي LC / MS / MS. توفر حساسية وانتقائية UPLC / MS / MS بمستويات اكتشاف منخفضة بيانات دقيقة وموثوقة يمكن استخدامها لمجموعة متنوعة من الأغراض ، بما في ذلك التحليلات الإحصائية للحرائك الدوائية.
4-4-تحديد كمية الشوائب
في صناعة الأدوية وعمليات الصياغة ، يشكل عزل وتحديد كمية المركبات الصيدلانية والشوائب في المواد الخام والمنتج النهائي جزءًا كبيرًا من البحث. يتطلب تحديد الشوائب باستخدام كروماتوغرافيا عالية الدقة عمليات فصل موثوقة وقابلة للتكرار وكشف جميع الشوائب المعروفة في المركب الصيدلاني النشط.
من المهم أيضًا تحديد كميات صغيرة من الشوائب بتركيزات عالية من المركب الطبي الفعال. على الرغم من أن هذا يصبح أكثر تعقيدًا في وجود المواد المضافة في العينة ، خاصةً في التحليل باستخدام أجهزة HPLC التقليدية ، فإن UPLC يوفر دقة أعلى للسماح بفصل واكتشاف كميات صغيرة من الشوائب.
5-4-عيوب UHPLC
سعر الجهاز والمعدات في هذه الطريقة أعلى من الكروماتوغرافيا. نظرًا لزيادة الضغط ، من الضروري إجراء صيانة أكثر دقة لمكونات الجهاز ، كما أن عمر العمود أقصر في هذه الطريقة. بالإضافة إلى ذلك ، لا يمكن استرجاع الأطوار الثابتة التي تقل عن µm2 وبالتالي فهي ليست فعالة من حيث التكلفة [6 ، 7]. في UPLC ، يمكن استخدام مضختين فقط (وليس 3 أو 4 مضخات). عدد المراحل الثابتة المستخدمة في هذا الجهاز محدود ، على الرغم من أن سرعة إنشاء مراحل ثابتة جديدة تتقدم. تشمل الجوانب السلبية الأخرى لـ UPLC الضغط الخلفي الأعلى من HPLC التقليدي ، والذي يمكن تقليله عن طريق رفع درجة حرارة العمود.
5-الخاتمة
حققت UPLC تقدمًا كبيرًا في مجالين من مجالات الكيمياء والأجهزة وأدت إلى الفصل والسرعة والحساسية العالية في الكروماتوغرافيا السائلة. عندما يواجه العديد من الباحثين عقبات في الفصل مع HPLC التقليدي ، يوفر UPLC الفرصة للتغلب على العقبات من خلال تطوير وزيادة كفاءة الكروماتوغرافيا. من المزايا المهمة لـ UPLC تقليل وقت التحليل ، مما يقلل بالتالي من استهلاك المذيبات. في الكروماتوغرافيا السائلة ، يعد وقت التحليل واستهلاك المذيبات وتكلفة التحليل مهمة في أي مختبر تحليلي ، لذا فإن تحسين الطريقة يؤدي إلى تقليل الوقت للوصول إلى توازن العمود. يمكن مقارنة الحساسية من خلال دراسة عرض الذروة بنصف ارتفاع ، والحساسية في UPLC أعلى بكثير من HPLC التقليدي.
المصادر والمراجع
۱ – F.K. Liu, Chromatographia 66 (2007) 791.
۲ – J.P.Wilcoxon, J.E. Martin, P. Provencio, Langmuir 16 (2000) 9912.
۳ – F.K. Liu, G.T.Wei, Chromatographia 59 (2004) 115.
۴ – G.T.Wei, F.K. Liu, J. Chromatogr. A 836 (1999) 253.
۵ – Y. Mori, M. Furukawa, T.Hayashi, K.Nakamura, Particul. Sci. Technol. 24 (2006)97.
۶ – P.M. Shiundu, S.M. Munguti, S.K.R. Williams, J. Chromatogr. A 983 (2003) 163.
۷ – J.C. Giddings, Science 260 (1993) 1456.
۸ – F.K. Liu, Chromatographia 66 (2007) 791.
۹ – F.K. Liu, G.T.Wei, Chromatographia 59 (2004) 115.
۱۰ – C.K. Lo, M.C. Paau, D. Xiao, M.M.F. Choi, Electrophoresis 29 (2008) 2330.
۱۱ – J.P.Wilcoxon, J.E. Martin, P. Provencio, J. Chem. Phys. 115 (2001) 998.
۱۲ – Y. Song, M.L.A.V. Heien, V. Jimenez, R.M.Wightman, R.W. Murray, Anal. Chem. 76 (2004) 4911.
۱۳ – Y. Song, V. Jimenez, C. McKinney, R. Donkers, R.W. Murray, Anal. Chem. 75 (2003) 5088.
۱۴ – V.L. Jimenez, M.C. Leopold, C. Mazzitelli, J.W. Jorgenson, R.W. Murray, Anal. Chem. 75 (2003) 199.
۱۵ – W. Bos, J.J. Steggerda, S. Yan, J.A. Casalnuovo, Inorg. Chem. 27 (1988) 948.
۱۶ – G. Schmid, ClustersColloids: Theory to Applica- tions, VCH, Weinhein, 1994.
۱۷ – A. Henglein, J. Phys. Chem. 97 (1993) 5457.
۱۸ – R.W. Devenish, T. Goulding, B.T. Heaton, R. Whyman, J. Chem. Soc., Dalton Trans. N5 (1996) 673.
۱۹ – K.A. Littau, P.J. Szajowski, A.R. Kortan, L.E. Brus, J. Phys. Chem. 97 (1993) 1224.
۲۰ – Ch.-F. Fischer, M. Giersigs, Langmuir 8 (1992) 1475.
۲۱ – T. Siebrands, M. Giersigs, P. Mulvaney, Ch.-F. Fischer, Langmuir 9 (1993) 2297.
۲۲ – J.J. Kirkland, J. Chromatogr. 185 (1979) 273.
۲۳ – Ch.-F. Fischer, M. Giersig, J. Chromatogr. A 688 (1994) 97.
۲۴ – Ch.-F. Fischer, M. Giersig, T. Siebrands, J. Chromatogr. A 670 (1994) 89.
۲۵ – A. Dass, R. Guo, J.B. Tracy, R. Balasubramanian, A.D. Douglas, R.W. Murray, Langmuir 24 (2008)
۲۶ – R.L.Wolfe, R.W. Murray, Anal. Chem. 78 (2006) 1167.
۲۷ – R. Balasubramanian, R. Guo, A.J. Mills, R.W. Murray, J. Am. Chem. Soc. 127 (2005) 8126.
۲۸ – V.L. Jimenez, D.G. Georganopoulou, R.J. White, A.S. Harper, A.J. Mills, D.I. Lee, R.W. Murray, Langmuir 20 (2004) 6864.
۲۹ – A.M. Al-Somali, K.M. Krueger, J.C. Falkner, V.L. Colvin, Anal. Chem. 76 (2004) 5903.
۳۰ – G.T. Wei, F-K. Liu, C.R.C. Wang, Anal. Chem. 71 (1999) 2085.
۳۱ – T. Okada, Anal. Chem. 60 )1988) 1511.
۳۲ – W. L. Hinze, In Ordered Media in Chemical Separation; Hinze, W. L., Armstrong, D. L., Eds.; ACS Symposium Series 342; American Chemical Society: Washington, DC, 1987; pp 2-82.
۳۳ – A. Berthod, I. Girard, C. Gonnet, In Ordered Media in Chemical Separation; Hinze, W. L., Armstrong, D. L., Eds.; ACS Symposium Series 342; American Chemical Society: Washington, DC, 1987; pp 130-141.
۳۴ – W. G. Tramposch, S.G. Weber, Anal. Chem. 58 (1986) 3006.
۳۵ – G.T. Wei, F-K. Liu, J. Chrom. A. 836 (1999) 253.

